химическое сродство
ХИМИЧЕСКОЕ СРОДСТВО (сродство реакции)
параметр термодинамич. системы, характеризующий отклонение от состояния хим. равновесия. Если реакцию записать в виде уравнения:
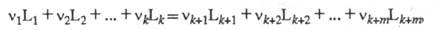
где L1, ..., Lk — исходные реагенты, Lk+1, ..., Lk+m — продукты реакции, v1, ..., vk и vk+1 , ..., vk+m — стехиометрич. коэф., то Х. с. А равно:
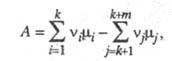
где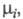
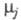 — хим. потенциалы соотв. исходных реагентов и продуктов. В состоянии равновесия
— хим. потенциалы соотв. исходных реагентов и продуктов. В состоянии равновесия
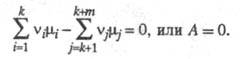
При A > 0 неравновесное состояние системы характеризуется избытком исходных реагентов и для достижения равновесия реакция должна идти слева направо; при А /i> 0, наоборот, система содержит избыток продуктов и реакция должна идти в противоположном направлении. Х. с. равно <i style="color:green">макс.</i> полезной работе реакции, взятой со знаком минус. Х. с. определяет собственно хим. процесс, связанный лишь с изменением состава системы и не связанный с работой по преодолению сил <i style="color:green">внеш.</i> давления <span style="color:green">(<i style="color:green">см.</i> <<максимальная работа реакции).
Единица измерения Х. с. — Дж/моль.
Стандартное Х. с. А0 определяется соотношением:
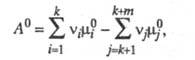
где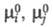 — стандартные хим. потенциалы соотв. реагентов и продуктов (см. стандартное состояние). Стандартное Х. с. связано со стандартным изменением энергии Гиббса
— стандартные хим. потенциалы соотв. реагентов и продуктов (см. стандартное состояние). Стандартное Х. с. связано со стандартным изменением энергии Гиббса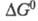 и константой равновесия реакции К:
и константой равновесия реакции К:
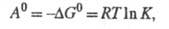
где Т — абс. температура; R — газовая постоянная.
В хим. термодинамике Х. с. рассматривается в сочетании с хим. переменной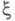 (наз. также степенью полноты реакции, числом пробегов реакции). Если в системе изменение чисел молей компонентов dni происходит лишь в результате хим. реакции (закрытая система), то dni связаны соотношением:
(наз. также степенью полноты реакции, числом пробегов реакции). Если в системе изменение чисел молей компонентов dni происходит лишь в результате хим. реакции (закрытая система), то dni связаны соотношением:
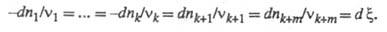
Интегрирование этого соотношения приводит к выражениям:
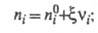
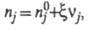
где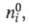
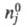 — соотв. числа молей исходных компонентов и продуктов в начальный момент времени. Эти выражения являются определяющими для хим. переменной
— соотв. числа молей исходных компонентов и продуктов в начальный момент времени. Эти выражения являются определяющими для хим. переменной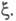 Энергия Гиббса системы
Энергия Гиббса системы
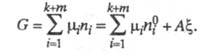
С помощью Х. с. и хим. переменной можно провести термодинамич. описание закрытой системы, где обратимо протекает химическая реакция, способом, отличным от традиционного описания Гиббса. Цель подобного описания — уменьшить число переменных ni, nj благодаря учету стехиометрии реакции. Полные дифференциалы термодинамических потенциалов такой системы — внутр. энергии U, энтальпии H, энергии Гиббса G, свободной энергии Гельмгольца F — м. б. представлены в виде формул:
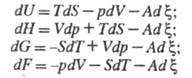
(S — энтропия системы; V — объем; р — давление). Отсюда следует:
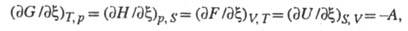
т. е. Х. с. является производной любого термодинамич. потенциала по хим. переменной при постоянстве естеств. переменных каждого из потенциалов. В этих выражениях член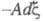 заменяет сумму
заменяет сумму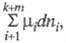 используемую при традиционном (Гиббсовом) описании. При этом вместо числа переменных (k + т) достаточно одной независимой переменной
используемую при традиционном (Гиббсовом) описании. При этом вместо числа переменных (k + т) достаточно одной независимой переменной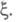 Если в системе протекает r независимых реакций, для описания системы нужно ввести r хим. переменных и r величин Х. с. Л.
Если в системе протекает r независимых реакций, для описания системы нужно ввести r хим. переменных и r величин Х. с. Л.
Х. с. и хим. переменную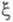 обычно относят к т. наз. внутренним параметрам макроскопич. системы. Это означает, что, во-первых, А и
обычно относят к т. наз. внутренним параметрам макроскопич. системы. Это означает, что, во-первых, А и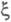 однозначно выражаются через параметры системы (хим. потенциалы, числа молей) и стехиометрич. коэф. и, во-вторых, A и
однозначно выражаются через параметры системы (хим. потенциалы, числа молей) и стехиометрич. коэф. и, во-вторых, A и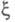 не характеризуют однозначно состояние термодинамич. равновесия (А = 0 для всех состояний равновесия). В термодинамике необратимых процессов величина А/Т рассматривается как обобщенная термодинамич. сила, а скорость хим. реакции
не характеризуют однозначно состояние термодинамич. равновесия (А = 0 для всех состояний равновесия). В термодинамике необратимых процессов величина А/Т рассматривается как обобщенная термодинамич. сила, а скорость хим. реакции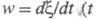 — время) — как обобщенный поток. Произведение (A/T)w обусловливает производство энтропии в системе вследствие хим. реакции. Вблизи состояния термодинамич. равновесия постулируется связь между w и А/Т типа:
— время) — как обобщенный поток. Произведение (A/T)w обусловливает производство энтропии в системе вследствие хим. реакции. Вблизи состояния термодинамич. равновесия постулируется связь между w и А/Т типа:
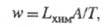
коэф. Lхим наз. хим. проводимостью.
Понятие Х. с. введено Т. де Донде в 1922.
Лит. см. при ст. термодинамика необратимых процессов, термодинамические потенциалы.
М. В. Коробов
Значения в других словарях
- Химическое сродство — Термин, применяющийся для характеристики способности данных веществ к химическому взаимодействию между собой или для характеристики степени устойчивости получающегося при этом соединения к разложению на исходные вещества. В разное время Х. Большая советская энциклопедия
- Химическое сродство — "Способность каждого простого тела соединяться с другими элементами и образовывать с ними сложные тела, в большей или меньшей степени склонные давать новые, сложнейшие соединения, составляет основной характер каждого элемента. Так, напр. Энциклопедический словарь Брокгауза и Ефрона
