янтарная кислота
ЯНТАРНАЯ КИСЛОТА (бутандиовая кислота) HOOC(CH2)2COOH
мол. м. 118,09; бесцветные кристаллы; т. пл. 108 °C; возгоняется при 140 °C/1–2 мм. рт.ст., 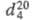 1,563;
1,563; 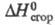 −1491,18 Дж/моль,
−1491,18 Дж/моль, 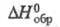 −940,35 Дж/моль; К1 6,89∙10−5, К22,47∙10−6 (вода, 25 °C); растворимость (в г в 100 мл растворителя): вода 5,8 (20 °C); 121 (100 °C), этанол 7,5 (21,5 °C), диэтиловый эфир 0,3 (15 °C), не раств. в бензоле, бензине, хлороформе.
−940,35 Дж/моль; К1 6,89∙10−5, К22,47∙10−6 (вода, 25 °C); растворимость (в г в 100 мл растворителя): вода 5,8 (20 °C); 121 (100 °C), этанол 7,5 (21,5 °C), диэтиловый эфир 0,3 (15 °C), не раств. в бензоле, бензине, хлороформе.
Я. к. обладает хим. свойствами, характерными для дикарбоновых кислот, образуя два ряда производных (табл.). Соли и эфиры Я. к. наз. сукцинатами.
СВОЙСТВА НЕКОТОРЫХ ПРОИЗВОДНЫХ ЯНТАРНОЙ КИСЛОТЫ
таблица в процессе добавления
* При 4 мм рт. ст. ** При 60 °C.
Я. к. содержится в небольшом количестве в буром угле, прир. смолах, в янтаре (отсюда название). Найдена во мн. растениях.
Конденсация Я. к. или ее эфиров с кетонами и альдегидами в присутствии оснований приводит к алкилиденянтарным кислотам (см. штоббе конденсация); при взаимодействии с аммиаком и аминами образуются сукцинимид и его N-замещенные производные; с ароматич. соед. в условиях реакции Фриделя — Крафтса -4-арил-4-кетомасляная кислота (реакция сукциноилирования). При окислении Я. к. H2O2 в зависимости от условий образуются пероксиянтарная (CH2COOОН)2, оксоянтарная или малоновая кислоты либо смесь ацетальдегида, малоновой и малеиновой кислот, при окислении KMnO4 — щавелевая кислота или смесь малоновой и винной кислот, при окислении NaClO4 — 3-гидроксипропионовая кислота, Каталитич. восстановление Я. к. в зависимости от катализатора и условий реакции приводит к 1,4-бутандиолу, 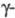 бутиролактону, ТГФ или к смеси этих соед., гидрирование в 1,4-бутандиоле — к
бутиролактону, ТГФ или к смеси этих соед., гидрирование в 1,4-бутандиоле — к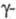 гидроксимасляной кислоте.
гидроксимасляной кислоте.
При 235 °C Я. к. отщепляет воду, давая янтарный ангидрид, при фотохим. распаде mpem-бутилпероксиэфиров — этилен.
Я. к. вступает в реакции замещения по активным метиленовым группам. Нагревание с бромом в закрытом сосуде при 100 °C дает с количеств. выходом 2,3-дибромянтарную кислоту.
Я. к. получают в качестве побочного продукта при производстве адипиновой кислоты, а также выделяют из смеси кислот, образующихся при окислении углеводородов C4 — C10. Я. к. может быть получена окислением фурфурола пероксидом водорода, гидрированием малеинового ангидрида с последующей гидратацией. Известен пром. способ выделения Я. к. из отходов янтаря.
Соли Я. к. образуются при окислении 1,4-бутандиола раствором Na2O2 или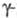 гидроксимасляной кислоты гидроксидами щел.-зем. металлов в присутствии Pd.
гидроксимасляной кислоты гидроксидами щел.-зем. металлов в присутствии Pd.
Применяют Я. к. для получения алкидных смол, сукцинатов, фотоматериалов, красителей, лек. веществ. Эфиры Я. к. используют в пищ. и парфюм. промышленности. Так, диэтилсукцинат — ароматизатор для пищ. продуктов, компонент парфюм. композиций (запах цветов); обладает также свойствами пластификатора. Моно- и диамиды Я. к. с ароматич. и гетероциклич. аминами применяют в производстве некоторых красителей и инсектицидов.
Для Я. к. ПДК в воде водоемов 0,01 мг/л.
Лит.: Kirk-Othmer encyclopedia, 3 ed., v. 21, N. Y., 1983, p. 848–64.
Н. Н. Магдесиева
Значения в других словарях
- Янтарная кислота — Этан-1,2-дикарбоновая кислота, HOOCCH2CH2COOH; бесцветные кристаллы, растворимые в спирте, эфире и воде tпл. 185° С, плотность 1,563 г/см3 (20 °С). Большая советская энциклопедия
- Янтарная кислота — Природная дикарбоновая кислота ациклического ряда, участвующая в цикле трикарбоновых кислот; применяется при изготовлении красителей, инсектицидов и некоторых лекарственных средств. Медицинская энциклопедия
- янтарная кислота — НООССН2СН2 СООН, дикарбоновая к-та. В свободном и связанном виде обнаружена в тканях растений и животных, в янтаре, буром угле и др. В больших кол-вах синтезируется при бактериальном разложении нек-рых органич. Биологический энциклопедический словарь
- ЯНТАРНАЯ КИСЛОТА — ЯНТАРНАЯ КИСЛОТА — НООС(СН2)2СООН, бесцветные кристаллы, Tпл 188 °С. Ее соли и эфиры называются сукцинатами. В небольших количествах содержится в янтаре, бурых углях и др. Применяют для получения синтетических смол, в органическом синтезе. Большой энциклопедический словарь
